
Sodyum karbonat ile sodyum bikarbonat arasındaki farklar neler?
Sodyum karbonat ve sodyum bikarbonat, kimyasal yapıları ve özellikleri bakımından farklılık gösteren iki önemli bileşiktir. Bu yazıda, her iki bileşiğin tanımları, kimyasal formülleri, asidik ve bazik özellikleri ile kullanım alanları ele alınmaktadır. Ayrıca, sağlık üzerindeki etkileri ve güvenlik önlemleri de vurgulanmaktadır.
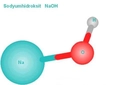
Sodyum Karbonat ve Sodyum Bikarbonat: Temel Tanımlar Sodyum karbonat (Na₂CO₃) ve sodyum bikarbonat (NaHCO₃), kimyasal bileşikler olarak önemli farklılıklara sahip olsalar da, genellikle birbirleriyle karıştırılmaktadırlar. Her iki bileşen de sodyum içermekte, ancak farklı kimyasal yapıları ve özellikleri bulunmaktadır. Kimyasal Yapıları ve Formülleri Sodyum karbonat, iki sodyum atomu, bir karbon atomu ve üç oksijen atomundan oluşur. Kimyasal formülü Na₂CO₃'tir. Sodyum bikarbonat ise bir sodyum atomu, bir hidrojen atomu, bir karbon atomu ve üç oksijen atomundan oluşur. Kimyasal formülü ise NaHCO₃'tür. Asidik ve Bazik Özellikler Sodyum karbonat, bazik bir bileşiktir ve su ile karıştığında alkali bir çözelti oluşturur. Bu nedenle, genellikle pH'ı artırmak için kullanılır. Sodyum bikarbonat ise hafif asidik özelliklere sahip bir bileşiktir. Su ile karıştığında, bikarbonat iyonları (HCO₃⁻) oluşturur ve bu da pH seviyesini düşürür. Bu özellik, sodyum bikarbonatın asidik ortamlarda antasit olarak kullanılmasını sağlar. Kullanım Alanları Sodyum karbonat ve sodyum bikarbonat, çeşitli endüstriyel ve günlük yaşamda farklı kullanım alanlarına sahiptir:
Fiziksel Özellikler Sodyum karbonat, beyaz toz halinde bulunur ve suda çözündüğünde alkalin bir çözeltinin oluşmasına neden olur. Genellikle "soda" olarak adlandırılan bu bileşik, yüksek sıcaklıklara dayanıklıdır. Sodyum bikarbonat ise beyaz kristal veya toz halinde bulunur ve suda çözünebilir. Bu bileşenin en belirgin özelliği, sıcaklık arttıkça karbondioksit gazı salınmasıdır. Bu özellik, sodyum bikarbonatın pişirme ve kabartma süreçlerinde önemli bir rol oynamasını sağlar. Sonuç Sodyum karbonat ve sodyum bikarbonat, kimyasal yapı, özellikler ve kullanım alanları bakımından önemli farklılıklar göstermektedir. Her iki bileşik de kendi özel uygulamalarında değerli olsalar da, kullanıcıların bu bileşenleri doğru bir şekilde ayırt edebilmeleri önemlidir. Yanlış kullanımlar, istenmeyen kimyasal tepkimelere ve ürünlerin beklenen etkilerini yitirmesine yol açabilir. Ekstra Bilgiler Sodyum karbonat ve sodyum bikarbonat, doğada doğal mineraller olarak da bulunabilmektedir. Sodyum karbonat, natron veya soda ash olarak adlandırılan doğal bir mineral formunda bulunurken, sodyum bikarbonat, natron adı verilen başka bir mineral formunda bulunabilir. Ayrıca, her iki bileşenin de insan sağlığı üzerindeki etkileri dikkate alınmalıdır; özellikle yüksek miktarda alındığında sağlık sorunlarına yol açabilirler. Bu nedenle, bu kimyasalların kullanımı sırasında dikkatli olunmalı ve ilgili güvenlik önlemleri alınmalıdır. |




.webp)


































Sodyum karbonat ve sodyum bikarbonat arasındaki farkları anladığım kadarıyla, bu iki bileşiğin kimyasal yapılarının yanı sıra fiziksel özellikleri ve kullanım alanları da oldukça farklı. Sodyum karbonatın bazik özellikleri nedeniyle su ile karıştığında alkali bir çözeltinin oluşması, onu pH artırıcı olarak kullanışlı kılıyor. Diğer yandan, sodyum bikarbonatın hafif asidik özellikleri, onu antasit olarak kullanmaya uygun hale getiriyor. Ayrıca, sodyum bikarbonatın pişirme ve kabartma süreçlerinde önemli bir rol oynadığını öğrenmek oldukça ilginçti. Bu iki bileşiğin birbirleriyle karıştırılması, istenmeyen kimyasal tepkimelere yol açabileceğinden doğru bir şekilde ayırt edilmesi gerektiği vurgulanmış. Bu durum, özellikle yemek yaparken veya temizlik ürünleri kullanırken dikkat edilmesi gereken bir nokta. Sodyum karbonatın cam üretimindeki rolü ve sodyum bikarbonatın mutfaktaki kabartma tozu olarak kullanımı gibi farklı alanlarda bu maddelerin kullanımını görmek, kimyanın günlük yaşamımızda ne kadar önemli bir yer tuttuğunu gösteriyor. Sonuç olarak, bu iki bileşiğin özelliklerini ve kullanımlarını bilmek, hem evde hem de sanayide daha bilinçli seçimler yapmamıza yardımcı olabilir. Peki, siz bu iki bileşiği kullanırken dikkat ettiğiniz özel bir durum ya da deneyim yaşadınız mı?
Sodyum Karbonat ve Sodyum Bikarbonatın Farkları
Sera, sodyum karbonat ve sodyum bikarbonat arasındaki farklara dikkat çektiğin için teşekkür ederim. Bu iki bileşiğin kimyasal ve fiziksel özellikleri, gerçekten de birçok alanda farklı işlevler üstlenmelerine olanak tanıyor. Sodyum karbonatın bazik özellikleri sayesinde pH artırıcı olarak kullanılması, su arıtma veya temizlik ürünlerinde sıkça tercih edilmesine yol açarken, sodyum bikarbonatın hafif asidik yapısı onun antasit olarak kullanılmasını sağlıyor.
Pişirme ve Temizlikte Kullanımları
Sodyum bikarbonatın pişirme sürecindeki rolü, kabartma tozunun temel bileşeni olması nedeniyle mutfakta oldukça yaygındır. Özellikle hamur işlerinde kabarma işlemini sağlarken, sodyum karbonatın cam üretimindeki rolü ise endüstriyel uygulamalarda önem taşıyor. Bu kullanım alanları, bu bileşiklerin günlük yaşamımızdaki etkisini gözler önüne seriyor.
Dikkat Edilmesi Gereken Noktalar
Söz konusu karıştırmalar olduğunda, özellikle yemek yaparken veya temizlik ürünleri kullanırken dikkatli olmak önemli. Yanlış bir bileşenin kullanılması istenmeyen kimyasal tepkimelere yol açabilir. Kendi deneyimime dayanarak, sodyum bikarbonatı kullanırken dikkat ettiğim bir durum, miktarını aşmamaktır; çünkü fazla kullanımı beklenmedik sonuçlar doğurabiliyor.
Bu bilgileri paylaşman, hem evde hem de sanayide doğru seçimler yapmamıza yardımcı oluyor. Senin de bu iki bileşiği kullanırken yaşadığın özel bir durum var mı?