
Sodyum su ile tepkimeye girdiğinde ne olur?
Sodyum ve su tepkimesi, sodyumun su ile etkileşimi sonucu meydana gelen şiddetli bir kimyasal reaksiyondur. Bu süreç, sodyum hidroksit ve hidrojen gazı üretirken, ekzotermik özellikleri nedeniyle ısı açığa çıkarır. Tepkimenin güvenli bir şekilde gerçekleştirilmesi için gerekli önlemler alınmalıdır.
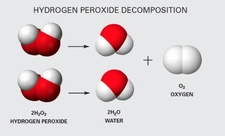
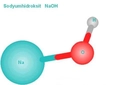
Sodyum ve Su Tepkimesi Sodyum, alkali metaller arasında yer alan ve oldukça reaktif bir elementtir. Sodyum, su ile tepkimeye girdiğinde oldukça şiddetli bir reaksiyon meydana gelir. Bu tepki, sodyumun elektron verme eğiliminden kaynaklanmaktadır ve bu durum, su molekülleri ile etkileşime girdiğinde belirgin bir şekilde ortaya çıkar. Tepkime Mekanizması Sodyum, su ile tepkimeye girdiğinde, aşağıdaki kimyasal denklemi oluşturur:\[ 2Na + 2H_2O \rightarrow 2NaOH + H_2 \uparrow \]Bu denklemde:- Na: Sodyumu temsil eder.- H2O: Su molekülünü temsil eder.- NaOH: Sodyum hidroksit, yani kostik soda olarak bilinen bir bileşiktir.- H2: Hidrojen gazı, tepkime sırasında açığa çıkan gazdır. Reaksiyon Ürünleri Sodyum ve su tepkimesinin ürünleri şunlardır:
Sodyum hidroksit, güçlü bir bazdır ve su ile tepkime sonucunda oluşan sodyum hidroksit çözeltisi, alkalin özelliklere sahiptir. Ayrıca, hidrojen gazı ise, bu tepkime sırasında açığa çıkar ve genellikle baloncuklar şeklinde gözlemlenir. Tepkimenin Özellikleri Bu tepkimenin birkaç önemli özelliği vardır:
Güvenlik ve Dikkat Edilmesi Gerekenler Sodyumun su ile tepkimesi son derece tehlikeli olabilir. Bu nedenle, bu tür deneylerin uygun güvenlik önlemleri alınarak ve laboratuvar ortamında gerçekleştirilmesi gerekmektedir. Dikkat edilmesi gereken hususlar şunlardır:
Sonuç Sodyum, su ile tepkimeye girdiğinde şiddetli bir reaksiyon meydana getirir ve bu süreçte sodyum hidroksit ve hidrojen gazı oluşur. Bu tepkimenin ekzotermik özellikleri ve açığa çıkan gazın tehlikeli doğası, dikkatli bir şekilde ele alınması gerektiğini göstermektedir. Sodyum ve su arasındaki bu etkileşim, kimya derslerinde sıklıkla anlatılan klasik bir deneydir ve alkali metallerin reaktivitesini gözlemlemek için önemli bir örnek teşkil eder. Ekstra Bilgiler Sodyum, doğada serbest halde bulunmaz; genellikle tuz formunda, yani sodyum klorür (NaCl) olarak bulunur. Ayrıca, alkali metaller grubunun diğer üyeleriyle (lityum, potasyum, rubidyum, sezyum) benzer reaktivite özelliklerine sahiptir. Bu metalin reaktivesi, periyodik tabloda yer alan atom numarasının artmasıyla birlikte artar. Bu nedenle, sodyumun su ile tepkimesi, kimyasal bağların ve elementlerin reaktivitesinin anlaşılmasında önemli bir rol oynamaktadır. |




.webp)


































Sodyum ve su tepkimesinin bu kadar şiddetli olmasının sebebi nedir? Sodyumun elektron verme eğilimi, su molekülleri ile etkileşime girdiğinde nasıl bir etki yaratıyor? Tepkime sırasında açığa çıkan hidrojen gazının patlayıcı özelliği ile ilgili daha fazla bilgi verebilir misin? Ayrıca, laboratuvar ortamında bu tür deneylerin güvenli bir şekilde nasıl yapılması gerektiği hakkında ne düşünüyorsun?
Sodyum ve Su Tepkimesinin Şiddeti
Sodyumun su ile tepkimesinin bu kadar şiddetli olmasının başlıca sebebi, sodyumun oldukça reaktif bir metal olmasıdır. Sodyum, elektron verme eğilimi yüksek bir elementtir. Su molekülleri ile etkileşime girdiğinde, sodyum atomu bir elektronunu suya verir. Bu süreç, sodyumun pozitif yüklü sodyum iyonuna dönüşmesine neden olurken, su molekülleri de hidrojen iyonu ve hidroksit iyonu oluşturur. Bu tepkime sırasında ortaya çıkan enerji, hidrojen gazının hızla salınmasına ve bu gazın patlayıcı bir özelliğe sahip olmasına yol açar.
Hidrojen Gazının Patlayıcı Özelliği
Tepkime sırasında açığa çıkan hidrojen gazı, havada çok hızlı bir şekilde yanabilen ve patlayıcı bir karışım oluşturabilen bir gazdır. Bu, hidrojenin oksijen ile birleşme eğilimi ve düşük ateşleme sıcaklığı ile ilgilidir. Bu nedenle, sodyum ve su tepkimesi sırasında oluşan hidrojen gazının birikmesi, patlama riskini artırır.
Laboratuvar Ortamında Güvenlik Önlemleri
Bu tür deneylerin laboratuvar ortamında güvenli bir şekilde yapılabilmesi için çeşitli önlemler alınmalıdır. Öncelikle, deneyin yapıldığı alanın iyi havalandırılması ve gerekli güvenlik ekipmanlarının (gözlük, eldiven, önlük) kullanılması önemlidir. Ayrıca, tepkimenin gerçekleşeceği malzemelerin ve miktarların dikkatlice hesaplanması, aşırı miktarda sodyum kullanılmaması gerekmektedir. Deney sırasında bir yangın veya patlama riski olabileceğinden, deneyin bir güvenlik kabini içinde gerçekleştirilmesi de önerilir. Bu şekilde, hem deneyin güvenliği sağlanır hem de olası kazaların etkileri minimize edilir.