Sodyum hidroksit ve su tepkimesi nasıl gerçekleşir?
Sodyum hidroksit (NaOH) ve su tepkimesi, kimyasal süreçlerin temelini oluşturan önemli bir reaksiyondur. Bu makalede, sodyum hidroksitin su ile etkileşimi sonucu meydana gelen iyonların oluşumu, tepkimenin mekanizması ve uygulama alanları detaylı bir şekilde incelenecektir.
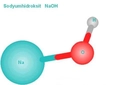
Sodyum Hidroksit ve Su Tepkimesi Nasıl Gerçekleşir?Sodyum hidroksit (NaOH), yaygın bir alkali bileşiktir ve su ile tepkimeye girdiğinde önemli kimyasal reaksiyonlar meydana gelir. Bu makalede, sodyum hidroksit ve su tepkimesinin temel mekanizmaları, ürünleri ve bu tepkimenin uygulamaları ele alınacaktır. Sodyum Hidroksit Nedir?Sodyum hidroksit, kimyasal formülü NaOH olan bir tuzdur. Genellikle beyaz, katı bir madde olarak bulunur ve suda iyi çözünebilen bir alkali madde olarak bilinir. Sanayide ve laboratuvarlarda yaygın olarak kullanılmasının yanı sıra, aynı zamanda güçlü bir kostik etkisi vardır. Su ve Sodyum Hidroksit Tepkimesi Sodyum hidroksit su ile karıştırıldığında, aşağıdaki tepkime gerçekleşir: NaOH (s) + H₂O (l) → Na⁺ (aq) + OH⁻ (aq) Bu tepkimede, sodyum hidroksit çözeltisi suda çözünerek sodyum iyonları (Na⁺) ve hidroksit iyonları (OH⁻) oluşturur. Bu iyonlar, çözeltinin pH seviyesini artırarak alkalin özellik kazandırır. Tepkimenin Mekanizması Tepkimenin mekanizması, sodyum hidroksit katı formunun su molekülleriyle etkileşime girmesiyle başlar. Su molekülleri, NaOH kristallerinin etrafında bir hidrasyon kabuğu oluşturarak iyonları serbest bırakır. Bu süreç, aşağıdaki adımlarla açıklanabilir:
Ürünler ve Özellikler Sodyum hidroksit ve su tepkimesinin ürünleri, sodyum iyonları ve hidroksit iyonlarıdır. Bu ürünler, aşağıdaki özelliklere sahiptir:
Uygulama Alanları Sodyum hidroksit ve su tepkimesi, çeşitli endüstriyel ve laboratuvar uygulamalarında önemli bir rol oynamaktadır:
Sonuç Sodyum hidroksit ve su tepkimesi, basit fakat önemli bir kimyasal reaksiyondur. Bu tepkime, sodyum hidroksitin su ile etkileşimi sonucunda güçlü alkalin özellikler kazandıran iyonları doğurur. Sodyum hidroksit, birçok endüstriyel ve laboratuvar uygulamasında kritik bir bileşen olarak öne çıkmaktadır. Bu nedenle, tepkimenin mekanizması ve ürünleri hakkında derinlemesine bilgi sahibi olmak, kimya alanında çalışanlar için büyük bir önem taşımaktadır. |




.webp)