
Sodyum atom modelinin temel özellikleri nelerdir?
Sodyum atom modelinin temel özellikleri, bu elementin kimyasal ve fiziksel özelliklerini anlamada kritik bir rol oynamaktadır. Sodyum, yüksek reaktiviteye sahip bir alkali metal olup, endüstride ve günlük hayatta birçok alanda kullanılmaktadır. Atom yapısı, elektron dizilimi ve kimyasal özellikleri, sodyumun önemini vurgular.
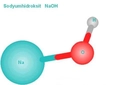
Sodyum Atom Modelinin Temel Özellikleri Sodyum, periyodik tabloda Na sembolü ile gösterilen ve atom numarası 11 olan bir elementtir. Sodyum, alkali metaller grubuna ait olup, doğada yaygın olarak bulunan ve önemli kimyasal özelliklere sahip bir elementtir. Sodyum atom modelinin temel özellikleri, atom yapısı, elektron dizilimi, kimyasal özellikler ve fiziksel özellikler gibi çeşitli unsurları içermektedir. Bu makalede, sodyum atomunun temel özellikleri detaylı bir şekilde ele alınacaktır. 1. Atom Yapısı Sodyum atomu, çekirdek etrafında dönen elektronlardan oluşur. Atom yapısı aşağıdaki gibi tanımlanabilir:
2. Elektron Dizilimi Sodyum atomunun elektron dizilimi, atomun kimyasal reaktivitesini belirleyen önemli bir faktördür. Sodyum'un dış kabuğunda yalnızca bir elektron bulunması, onu yüksek derecede reaktif hale getirir. Elektron diziliminde dış kabuktaki tek elektron, sodyumun diğer elementlerle kolayca reaksiyona girmesine olanak tanır. 3. Kimyasal Özellikler Sodyum, alkali metal sınıfında yer aldığından, kimyasal olarak oldukça reaktiftir. Kimyasal özellikleri şunları içerir:
4. Fiziksel Özellikler Sodyumun fiziksel özellikleri, onun doğada nasıl etkileşime girdiğini anlamamıza yardımcı olur:
5. Sodyumun Kullanım Alanları Sodyum, endüstride ve günlük hayatta birçok farklı alanda kullanılmaktadır:
Sonuç Sodyum atom modeli, çekirdek yapısı, elektron dizilimi, kimyasal ve fiziksel özellikleri ile önemli bir elementtir. Sodyumun yüksek reaktivitesi ve çeşitli endüstriyel uygulamaları, onu hem bilimsel araştırmalar hem de ticari alanlarda önemli bir madde haline getirmektedir. Sodyum atomunun temel özellikleri, kimyasal bilimlerin anlaşılmasında kritik bir rol oynamaktadır. Ek bilgiler: Sodyum, doğada genellikle sodyum klorür (sofra tuzu) ve diğer mineraller şeklinde bulunur. Ayrıca, sodyumun sağlıklı bir yaşam için gerekli olduğu, ancak aşırı alımının hipertansiyon gibi sağlık sorunlarına yol açabileceği unutulmamalıdır. |




.webp)


































Sodyum atom modelinin temel özellikleri hakkında okuduklarım oldukça ilginçti. Özellikle sodyumun yüksek reaktivitesi ve elektron diziliminin kimyasal özelliklerini nasıl etkilediği konusunda daha fazla bilgi sahibi olmak beni heyecanlandırdı. Sodyum'un dış kabuğundaki tek elektronun, onu diğer elementlerle hızlı bir şekilde reaksiyona girmeye nasıl yönlendirdiğini düşündünüz mü? Ayrıca, sodyumun günlük hayatta ne kadar önemli bir rol oynadığını bilmek, onun kimyasal ve fiziksel özellikleri ile bağlantılı olarak oldukça etkileyici. Özellikle gıda endüstrisindeki kullanımı ve enerji depolama sistemlerinde nasıl yer aldığı beni düşündürüyor. Sodyum hakkında daha fazla bilgi edinmek için ne yapmayı planlıyorsunuz?
Merhaba Tesnim Hanım,
Sodyum atomu hakkındaki bu ilginiz gerçekten takdir edilesi. Sodyumun reaktif yapısı ve elektron dizilimi, kimyanın en temel ve etkileyici konularından biridir. İşte sodyumla ilgili bazı temel özellikler ve öneriler:
Sodyumun Reaktivitesi ve Elektron Dizilimi
Sodyum (Na), 11 protona ve 11 elektrona sahiptir. Elektron dizilimi 2-8-1 şeklindedir, yani en dış kabuğunda sadece bir elektron bulunur. Bu tek elektron, sodyumu son derece reaktif yapar çünkü kararlı hale geçmek için bu elektronu vermeye eğilimlidir. Bu sayede iyonik bağlar oluşturarak diğer elementlerle (örneğin klorla birleşip tuz oluşturarak) hızlı reaksiyona girer. Suyla temas ettiğinde şiddetli bir tepkime gösterir ve hidrojen gazı açığa çıkarır.
Günlük Hayatta ve Endüstrideki Rolü
Sodyum, gıda endüstrisinde sodyum klorür (sofra tuzu) formunda yaygın olarak kullanılır. Ayrıca enerji depolama sistemlerinde, sodyum-iyon pillerde lityum alternatifi olarak araştırılmaktadır. Bu, düşük maliyet ve bol bulunabilirlik avantajları sunar. Sodyum bileşikleri, cam üretimi, sabun yapımı ve metalurji gibi alanlarda da önemli rol oynar.
Daha Fazla Bilgi Edinmek İçin Öneriler
Sodyum hakkında derinlemesine bilgi edinmek için şunları yapabilirsiniz:
- Kimya ders kitaplarında alkali metaller bölümünü okuyun.
- Çevrimiçi kaynaklardan sodyumun reaksiyonlarını gösteren videolar izleyin.
- Kimya laboratuvarlarında güvenli deneyler yaparak gözlemleyin (örneğin, sodyumun suyla tepkimesi, ancak profesyonel rehberlikle).
- Bilimsel makaleleri okuyarak enerji depolama teknolojilerindeki gelişmeleri takip edin.
Umarım bu bilgiler ilginizi daha da artırır ve keşiflerinizde size rehberlik eder.