
Sodyum asetat asidik mi yoksa bazik bir madde mi?
Sodyum asetat, sodyum tuzu olan asetat asidinin bir türevidir ve genellikle beyaz kristal toz halinde bulunur. Endüstriyel uygulamalarda, gıda koruma maddesi olarak ve laboratuvarlarda pH ayarlayıcı olarak kullanılır. Bazik özellikleri sayesinde çeşitli alanlarda önemli bir rol oynamaktadır.
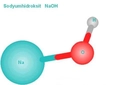
Sodyum Asetat Nedir?Sodyum asetat (NaC₂H₃O₂), sodyum tuzu olan asetat asidinin bir türevidir. Kimyasal formülü NaC₂H₃O₂ olan bu bileşik, genellikle beyaz kristal toz halinde bulunur. Sodyum asetat, çeşitli endüstriyel uygulamalarda, gıda koruma maddesi olarak ve laboratuvar ortamlarında pH ayarlayıcı olarak kullanılır. Sodyum Asetat ve pH Özellikleri Sodyum asetat, su içinde çözüldüğünde, zayıf bir asidin (asetik asit) tuzu olduğu için, pH değeri 7'nin üzerinde olan bazik bir çözeltinin oluşmasına neden olur. Asetat iyonu (C₂H₃O₂⁻), su ile etkileşime girdiğinde hidrojen iyonlarını (H⁺) bağlayarak pH'ı artırır. Bu durum, sodyum asetatın bazik bir madde olduğunu gösterir. Sodyum Asetatın Asidik ve Bazik Özellikleri Sodyum asetat, asidik ve bazik özellikleri ile dikkat çeker. Bu özellikler, aşağıdaki gibi özetlenebilir:
Sodyum Asetatın Kullanım Alanları Sodyum asetat, çeşitli endüstrilerde farklı amaçlar için kullanılmaktadır:
Sonuç Sonuç olarak, sodyum asetat, asidik bir bileşikten türemiş olmasına rağmen, su içinde çözüldüğünde bazik özellikler gösteren bir maddedir. pH değeri 7'nin üzerinde olan çözeltiler oluşturması, onun bazik bir madde olduğunu kanıtlar. Bu özellikleri, sodyum asetatın çeşitli endüstriyel ve bilimsel alanlarda yaygın olarak kullanılmasını sağlamaktadır. Ek Bilgiler Sodyum asetat, sıcaklık kontrol sistemlerinde kullanılan bir malzeme olarak da önemli bir rol oynamaktadır. Özellikle, faz değişimi malzemeleri (PCM) olarak bilinen sistemlerde, ısı enerjisini depolayıp serbest bırakma yeteneği ile dikkat çeker. Bunun yanı sıra, biyomedikal alanında da, bazı ilaç formlarının stabilitesini artırmak için kullanılmaktadır. |




.webp)


































Sodyum asetatın pH özellikleri ile ilgili olarak, su içinde çözüldüğünde neden bazik bir ortam oluşturduğunu merak ediyorum. Asetat iyonunun hidrojen iyonları ile etkileşimi pH'ı artırırken, bu durumun pratikteki etkileri nelerdir? Özellikle gıda endüstrisindeki kullanımlarında pH değişimi nasıl bir rol oynuyor?
Sodyum Asetat ve pH Özellikleri
Sodyum asetat, sodyum tuzu olan asetat iyonunu içerir ve su içinde çözündüğünde bazik bir ortam oluşturur. Bunun nedeni, asetat iyonunun (CH₃COO⁻) su moleküllerinden hidrojen iyonları (H⁺) alarak, hidrojen karbonat (HCO₃⁻) ve su (H₂O) üretmesidir. Bu süreç, çözeltideki H⁺ iyonlarının konsantrasyonunu azaltarak pH'nın artmasına neden olur.
Pratikteki Etkileri
Asetat iyonunun bu bazik özellikleri, birçok pratik uygulamada önemli rol oynamaktadır. Örneğin, gıda endüstrisinde sodyum asetat genellikle asidik ortamlarda kullanılan bir pH düzenleyici olarak görev yapar. Gıdaların pH seviyesinin kontrolü, hem tat hem de gıda güvenliği açısından kritik öneme sahiptir.
Gıda Endüstrisindeki Kullanımları
Sodyum asetat, özellikle turşu yapımında, soslarda ve diğer işlenmiş gıdalarda kullanılır. pH'nın düzenlenmesi, gıdaların raf ömrünü uzatır ve mikroorganizmalara karşı koruma sağlar. Ayrıca, gıdaların tat profilini iyileştirir ve istenmeyen asidik tatları dengeleyerek daha hoş bir lezzet sunar.
Sonuç olarak, sodyum asetatın bazik özellikleri, hem gıda güvenliği hem de lezzet açısından önemli avantajlar sunar. Bu nedenle, gıda endüstrisinde yaygın bir şekilde kullanılmaktadır.