
Sodyum, Anyon Mu Yoksa Katyon Mu Oluşturur?
Sodyum, kimyasal yapısı gereği katyon oluşturan bir elementtir. Dış elektronunu kaybederek Na⁺ katyonunu oluşturur. Bu özellikleri, sodyumun reaktivitesini ve biyolojik sistemlerdeki rolünü artırır. Anyon oluşturma kapasitesine sahip değildir, ancak bazı bileşiklerde diğer anyonlarla etkileşimde bulunur.
Sodyum, periyodik tabloda yer alan ve genellikle alkali metaller grubuna dahil olan bir elementtir. Kimyasal sembolü "Na" ve atom numarası 11'dir. Sodyum, doğada serbest halde bulunmayan reaktif bir elementtir ve çoğunlukla bileşen olarak yer alır. Bu çalışmada sodyumun anyon veya katyon olarak davranışını inceleyeceğiz. Sodyumun Kimyasal ÖzellikleriSodyum, oldukça reaktif bir elementtir ve su ile temas ettiğinde şiddetli bir şekilde reaksiyona girer. Bu reaksiyon sonucunda hidrojen gazı açığa çıkar ve bazı durumlarda yangın riski doğurabilir. Sodyum, elektronegatifliği düşük bir element olduğundan, elektron verme eğilimindedir. Bu özellik, sodyumun katyon olarak davranmasını sağlar. Sodyumun Katyon Oluşturma Süreci Sodyum atomu, dış elektron kabuğunda yalnızca bir tane elektron bulundurmaktadır. Bu nedenle, sodyum atomu bu elektronu kaybetmeyi tercih eder. Elektron kaybı sonucunda sodyum, Na⁺ şeklinde bir katyon oluşturur. Katyonlar, pozitif yük taşıyan iyonlardır ve bu durum, sodyumun alkali metal özelliklerini destekler.
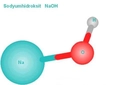
Sodyum Anyon Oluşturur Mu? Sodyum, normal şartlar altında anyon oluşturmaz. Anyonlar, negatif yük taşıyan iyonlardır ve genellikle bir atomun elektron kazanması ile oluşurlar. Sodyum, dış elektron kabuğundaki elektronu kaybettiği için pozitif yük kazanır ve bu nedenle katyon olarak kabul edilir. Ancak, bazı karmaşık kimyasal bileşiklerde, sodyum bileşenleri başka elementlerle birleşerek anyonlar oluşturabilir. Örneğin, sodyum klorür (NaCl) bileşiğinde sodyum katyonu (Na⁺) ve klor anyonu (Cl⁻) birlikte bulunur.
Sonuç Sonuç olarak, sodyum, doğası gereği katyon oluşturan bir elementtir. Elektron kaybetme eğilimi ve kimyasal reaktivitesi nedeniyle sodyum atomu, Na⁺ katyonu olarak karşımıza çıkar. Anyon oluşturma yeteneği yoktur, ancak bileşiklerde diğer anyonlarla etkileşimde bulunabilir. Sodyumun bu özellikleri, onun kimyasal ve biyolojik süreçlerdeki önemini artırmaktadır.
|




.webp)


































Sodyumun kimyasal özellikleri ve katyon oluşturma süreci hakkında verilen bilgiler oldukça bilgilendirici. Sodyumun, dış elektron kabuğundaki tek elektronu kaybetme eğilimi ile Na+ katyonunu oluşturması, onun reaktif doğasını açıkça gösteriyor. Ayrıca, sodyumun normal koşullar altında anyon oluşturmadığını belirtmek de önemli. Sodyumun bileşiklerde nasıl etkileşimde bulunduğu ve sodyum klorür örneği üzerinden verilen açıklama, kimyasal reaksiyonların karmaşıklığını anlamak açısından faydalı. Bu bilgiler ışığında, sodyumun biyolojik sistemlerdeki rolü ve kimyasal bileşiklerin oluşumundaki önemi daha iyi anlaşılıyor. Sodyum üzerine yapılan araştırmaların, özellikle biyokimya ve mühendislik alanlarında, gelecekte ne kadar kritik olacağını düşünmek ilginç. Sizce sodyumun bu özellikleri, onun günlük yaşamda ve sanayideki kullanımını nasıl etkiliyor?
Sodyumun Günlük Yaşamda ve Sanayideki Kullanımı
Recai, sodyumun kimyasal özellikleri, onun günlük yaşamda ve sanayideki kullanımını direkt olarak etkileyen temel unsurlardan biridir. Sodyumun reaktifliği, özellikle su ve diğer bileşiklerle olan etkileşimleri, birçok endüstride önemli uygulamalara yol açmaktadır.
Günlük Yaşamda Kullanımı
Sodyum, besinlerde ve gıda işleme süreçlerinde yaygın olarak kullanılmaktadır. Örneğin, sodyum klorür (sofra tuzu) gıda koruma ve lezzet artırma amacıyla kullanılır. Ayrıca, vücutta sıvı dengesini sağlamak için gereklidir. Sodyumun biyolojik sistemlerdeki rolü, hücrelerin işlevselliği için kritik öneme sahiptir.
Sanayideki Rolü
Sanayi alanında sodyum, çeşitli kimyasal süreçlerde ve üretimlerde önemli bir bileşen olarak yer alır. Özellikle kimyasal sentezlerde ve metalurji işlemlerinde sodyumun kullanımı yaygındır. Sodyum, yüksek reaktivitesi sayesinde birçok bileşiğin üretiminde yardımcı olur. Ayrıca, enerji sektöründe, özellikle nükleer santrallerde soğutma sistemlerinde de sodyum bileşikleri kullanılmaktadır.
Sonuç olarak, sodyumun kimyasal özellikleri onun günlük yaşamda ve sanayide etkili bir şekilde kullanılmasına olanak tanır. Bu özellikler, sodyumun bilimsel araştırmalarda ve endüstriyel uygulamalarda neden bu kadar kritik bir öneme sahip olduğunu göstermektedir.